Спектроскопическое иквантовохимическое исследованиеводородной связи и N:N взаимодействия молекулы мета-нитроанилина
Санжаров Николай Александрович
Томский государственный университет
Научный руководитель: Морозова Юлия Петровна, к.ф.-м.н
Исследование межмолекулярныхвзаимодействий между молекулами растворенного вещества и растворителяимеет большое теоретическое и прикладноезначение. С прикладной точкизрения важность определяется тем, что многиепромышленные технологии основаны на использовании веществ вжидкой фазе. С жидкой фазойсвязаны биологические, фотобиологические ифотохимические процессы.Особый интерес для практики имеютмногокомпонентные системы.Использование смешанных растворителей позволяетподобрать растворители так, чтомы можем исследовать любой вид межмолекулярного взаимодействия,так как каждый растворитель обладаетиндивидуальнымифизико-химическими свойствами, то есть, можно сказать,что с помощью смешанныхрастворителей возможнопрогнозированиеспектрально-люминесцентныхсвойств молекул, а также моделированиеразличных типоввзаимодействий для исследуемой молекулы. Откликполос поглощения намежмолекулярные взаимодействия позволяетполучать информацию о составесольватной оболочки в бинарномрастворителе. В нашемслучае состав сольватной оболочки определяется посдвигу полосы поглощения D
n
данной молекулы всмешанном растворителе различнойконцентрации. Используяизвестные выражения для энергии основного ивозбужденного состояния молекулы для процесса поглощения света,получаем выражение для полосыпоглощения: 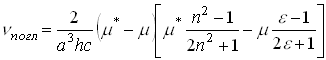  , где а - радиус полости, в которой находится молекула, h-постоянная Планка, с- скорость света, m
и m
*- дипольные моменты молекулыв основном и возбужденномсостояниях соответственно, n- показательпреломления, e
-диэлектрическаяпроницаемость. Применяя этуформулу для растворителей с n1 и n2, e
1 и e
2 в приближении,что n1»
n2»
n и a1»
a2»
a, получаем формулудля сдвига полосы поглощения: , где а - радиус полости, в которой находится молекула, h-постоянная Планка, с- скорость света, m
и m
*- дипольные моменты молекулыв основном и возбужденномсостояниях соответственно, n- показательпреломления, e
-диэлектрическаяпроницаемость. Применяя этуформулу для растворителей с n1 и n2, e
1 и e
2 в приближении,что n1»
n2»
n и a1»
a2»
a, получаем формулудля сдвига полосы поглощения: . Этот сдвиг обусловлен только универсальнымивзаимодействиями, а нам нужно учесть испецифическиевзаимодействия, поэтому формула примет вид: . Этот сдвиг обусловлен только универсальнымивзаимодействиями, а нам нужно учесть испецифическиевзаимодействия, поэтому формула примет вид:  . Из формулы видно, чтоуниверсальные взаимодействиязависят от разницы дипольных моментов восновном и возбужденномсостояниях. Для описания D
n
спец предложить выражения нет возможности,но D
n
спец можнооценить экспериментально. Длявозможности исследования этого сдвигатакже необходимо, чтобы былазначительная разница дипольных моментовв исследуемых состояниях.Именно из-за значительной разницы дипольныхмоментов m
и m
* дляисследования была выбранамолекула мета-нитроанилина (МНА). Для этоймолекулы были полученыхарактеристики электронных переходов методом ЧПДП[1]. D
n
спец для МНАможно представить в следующемвиде: . Из формулы видно, чтоуниверсальные взаимодействиязависят от разницы дипольных моментов восновном и возбужденномсостояниях. Для описания D
n
спец предложить выражения нет возможности,но D
n
спец можнооценить экспериментально. Длявозможности исследования этого сдвигатакже необходимо, чтобы былазначительная разница дипольных моментовв исследуемых состояниях.Именно из-за значительной разницы дипольныхмоментов m
и m
* дляисследования была выбранамолекула мета-нитроанилина (МНА). Для этоймолекулы были полученыхарактеристики электронных переходов методом ЧПДП[1]. D
n
спец для МНАможно представить в следующемвиде:  , где D
n
1 и D
n
2-сдвиги полос, обусловленныеспецифическими взаимодействиямиводородной связи нааминогруппе и на нитрогруппе соответственно, а D
n
3- сдвиг полосыпоглощения, обусловленный N...Nвзаимодействием. Составляющую D
n
спец можно промоделироватьдобавкой второй компоненты внеполярный растворитель. В качествевторой компоненты были выбранынитрометан и изопропанол. Придобавлении нитрометанапредполагалось оценить D
n
3. Былиизучены изменения в электронном спектрепоглощения МНА в гексане придобавлении нитрометана в области p
®
p
*электронных переходов (200-380 нм).При добавке нитрометана для полосы S0®
S1 МНАпроисходит изменение оптической плотности.В области второй полосыМНА имеет добавочное поглощение, подлине волны близкое к поглощению S0®
S2МНА, оптическая плотностькоторого возрастает с течением времени. Придобавке нитрометана в растворепроисходит выделение комплекса. Этообразующееся соединение,снятое в гексане, имеет следующие характеристики: S0®
S1- 342.5 нм и S0®
S2- 264.5 нм, отсюда виден сдвиг всторону меньших длин волн по сравнению схарактеристиками МНА вгексане (S0®
S1-344 нм и S0®
S2- 272 нм), при этом наблюдаются характерные измененияформы полосы. В начальный момент S0®
S2 имел формуплеча, а S0®
S1 был четким переходом, стечением времени картина меняется на обратную. Выделенный комплекс(нитрометан и МНА в гексане) был снят вэтаноле. В этом случае спектрстановился более сложным. При расшифровкеэтого спектра получилиследующие длины волн поглощения: 255 нм, 284 нм, 368 нм. Перваяиз них принадлежит p
p
* переходу нитробензола,вторая- полоса комплекса, сдвинутая поотношению к комплексу в гексанев сторону больших длин волн, третьяпринадлежит МНА в этаноле. Вероятно, вторая полоса принадлежит N...Nвзаимодействию азотааминогруппы МНА и азота нитрогруппы нитрометана. На основерассчитанных данных геометриимета-нитроанилина и нитрометанаквантовохимическим методомЧПДП был проведен расчет комплексамета-нитроанилин - нитрометан.Теперь перейдем к обсуждению проявления водороднойсвязи нитрогруппы МНА смолекулами спирта. К раствору молекулы МНА втетрахлорметане добавлялсяизопропанол так, что общий объем раствора составлял 5 см3,при этом концентрация МНА оставаласьпостоянной. При добавлении спирта, изменяя диэлектрическуюпроницаемость смеси, получаемсмещение полос поглощения МНА и изменение локальнойдиэлектрической проницаемоcти , где D
n
1 и D
n
2-сдвиги полос, обусловленныеспецифическими взаимодействиямиводородной связи нааминогруппе и на нитрогруппе соответственно, а D
n
3- сдвиг полосыпоглощения, обусловленный N...Nвзаимодействием. Составляющую D
n
спец можно промоделироватьдобавкой второй компоненты внеполярный растворитель. В качествевторой компоненты были выбранынитрометан и изопропанол. Придобавлении нитрометанапредполагалось оценить D
n
3. Былиизучены изменения в электронном спектрепоглощения МНА в гексане придобавлении нитрометана в области p
®
p
*электронных переходов (200-380 нм).При добавке нитрометана для полосы S0®
S1 МНАпроисходит изменение оптической плотности.В области второй полосыМНА имеет добавочное поглощение, подлине волны близкое к поглощению S0®
S2МНА, оптическая плотностькоторого возрастает с течением времени. Придобавке нитрометана в растворепроисходит выделение комплекса. Этообразующееся соединение,снятое в гексане, имеет следующие характеристики: S0®
S1- 342.5 нм и S0®
S2- 264.5 нм, отсюда виден сдвиг всторону меньших длин волн по сравнению схарактеристиками МНА вгексане (S0®
S1-344 нм и S0®
S2- 272 нм), при этом наблюдаются характерные измененияформы полосы. В начальный момент S0®
S2 имел формуплеча, а S0®
S1 был четким переходом, стечением времени картина меняется на обратную. Выделенный комплекс(нитрометан и МНА в гексане) был снят вэтаноле. В этом случае спектрстановился более сложным. При расшифровкеэтого спектра получилиследующие длины волн поглощения: 255 нм, 284 нм, 368 нм. Перваяиз них принадлежит p
p
* переходу нитробензола,вторая- полоса комплекса, сдвинутая поотношению к комплексу в гексанев сторону больших длин волн, третьяпринадлежит МНА в этаноле. Вероятно, вторая полоса принадлежит N...Nвзаимодействию азотааминогруппы МНА и азота нитрогруппы нитрометана. На основерассчитанных данных геометриимета-нитроанилина и нитрометанаквантовохимическим методомЧПДП был проведен расчет комплексамета-нитроанилин - нитрометан.Теперь перейдем к обсуждению проявления водороднойсвязи нитрогруппы МНА смолекулами спирта. К раствору молекулы МНА втетрахлорметане добавлялсяизопропанол так, что общий объем раствора составлял 5 см3,при этом концентрация МНА оставаласьпостоянной. При добавлении спирта, изменяя диэлектрическуюпроницаемость смеси, получаемсмещение полос поглощения МНА и изменение локальнойдиэлектрической проницаемоcти
Список публикаций:
1. Кузнецова И.В., Санжаров Н. А. Определениесостава сольватной оболочки молекул пара- имета- нитроанилинов в бинарныхрастворителях. Тезисы докладов ВНКСФ-6ассоциации студентов-физиков и молодых ученых России.Екатеринбург-Томск, 2000. С. 224.
|
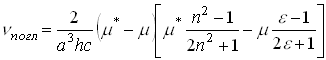
 . Этот сдвиг обусловлен только универсальнымивзаимодействиями, а нам нужно учесть испецифическиевзаимодействия, поэтому формула примет вид:
. Этот сдвиг обусловлен только универсальнымивзаимодействиями, а нам нужно учесть испецифическиевзаимодействия, поэтому формула примет вид:  . Из формулы видно, чтоуниверсальные взаимодействиязависят от разницы дипольных моментов восновном и возбужденномсостояниях. Для описания D
n
спец предложить выражения нет возможности,но D
n
спец можнооценить экспериментально. Длявозможности исследования этого сдвигатакже необходимо, чтобы былазначительная разница дипольных моментовв исследуемых состояниях.Именно из-за значительной разницы дипольныхмоментов m
и m
* дляисследования была выбранамолекула мета-нитроанилина (МНА). Для этоймолекулы были полученыхарактеристики электронных переходов методом ЧПДП[1]. D
n
спец для МНАможно представить в следующемвиде:
. Из формулы видно, чтоуниверсальные взаимодействиязависят от разницы дипольных моментов восновном и возбужденномсостояниях. Для описания D
n
спец предложить выражения нет возможности,но D
n
спец можнооценить экспериментально. Длявозможности исследования этого сдвигатакже необходимо, чтобы былазначительная разница дипольных моментовв исследуемых состояниях.Именно из-за значительной разницы дипольныхмоментов m
и m
* дляисследования была выбранамолекула мета-нитроанилина (МНА). Для этоймолекулы были полученыхарактеристики электронных переходов методом ЧПДП[1]. D
n
спец для МНАможно представить в следующемвиде: