|
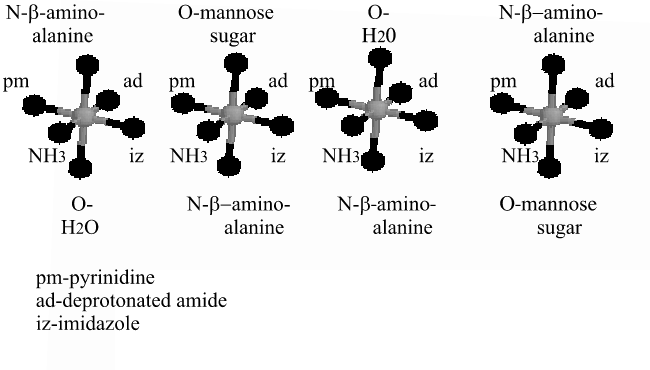
Локальная структура Fe(II)-блеомицина вокруг атома металла Ростовский государственный университет Научный руководитель: Солдатов Александр Владимирович, Доктор физико-математических наук Блеомицин - антибиотик, который используют для лечения различных опухолей. Одной из его форм является Fe(II)-блеомицин (Fe(II)-Bl), в котором ион Fe находится в высокоспиновом состоянии. Структура Fe(II)-Bl была исследована мало. До сих пор нет данных ни рентгеновской диффракции ни ЯМР в сочетании с расчетами методом молекулярной динамики. Однако, ранее был предложен ряд моделей для аналогичного комплекса Co(II)-блеомицина (Co(II)-Bl). Общим в них является наличие четырех лигандов железа, расположенных в одной плоскости: атомов азота пиримидина, имидозольного кольца, первичного и вторичного аминов. Различия же связаны с большой неопределенностью при выяснении того, какие лиганды и с какой стороны аксиально присоединяются к металлу. Схематично модели приведены (рис. 1).
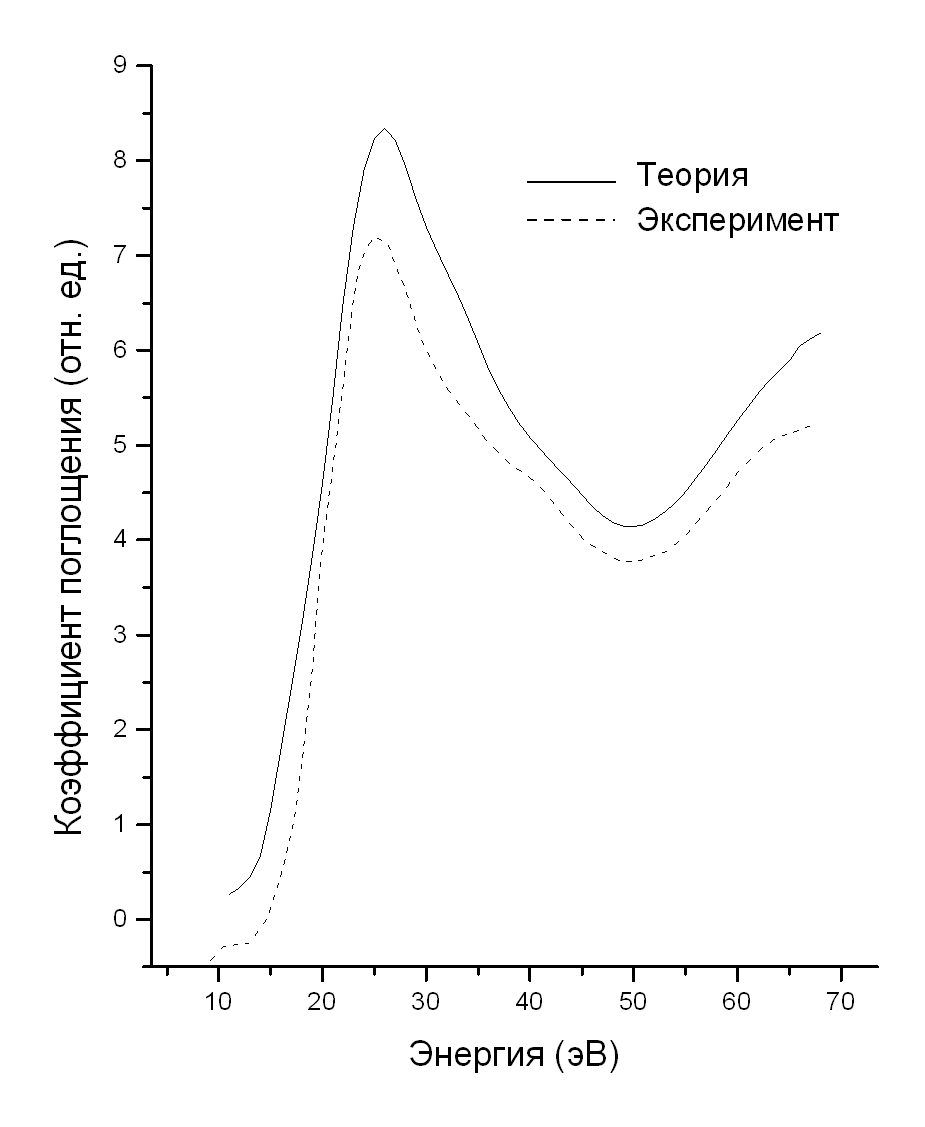
рис.1 Нами были проведены теоретические расчеты K- XANES спектров железа в Fe(II)-Bl с использованием этих моделей в формализме многократного рассеяния. Расчеты выполнены в кластере, состоящим из 20 атомов, ближайших к иону металла. Сопоставление формы теоретических спектров с экспериментальным позволило выбрать из предложенных моделей наиболее вероятную. В ней, в соответствии с выбором ориентации активного центра (рис. 1), нижний лиганд -азот
рис.2 |
| (c) АСФ России, 2001 |