|
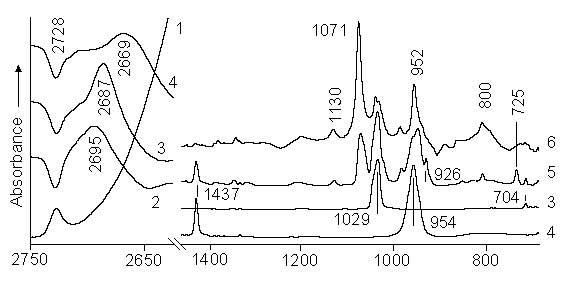
Исследование поверхности пористого льда методом инфракрасной спектроскопии Санкт-Петербургский государственный университет Научный руководитель: Цыганенко Алексей Алексеевич, д.ф-м.н. Гетерогенные процессы на поверхности льда играют значительную роль в химии атмосферы. Полагают, что на ледяных частицах происходят реакции, приводящие к уменьшению концентрации озона. В связи с этим необходимо исследование свойств дисперсного льда, адсорбции и реакций с участием озона на его поверхности. Попытки исследования адсорбции на поверхности льда с применением ИК-спектроскопии предпринимались и ранее [1-4]. В спектрах пленок льда, нанесенных на металлическое зеркало или прозрачную подложку, удалось наблюдать полосы свободных от водородной связи групп OH или OD и видеть их изменения при адсорбции молекул HCl, CCl 4 [1], NOx[2], CO [3,4]. Однако работ по адсорбции озона или изучению реакций с его участием известно не было. Восполнить этот пробел стало целью данной работы.В нашей работе пленка льда получалась на охлаждаемых жидким азотом внутренних окнах описанной ранее [5] кюветы. Вода выделялась из помещенных между окнами гранул цеолита, предварительно насыщенных водой, при их нагревании электрической спиралью, и, осаждаясь под косым углом на холодной поверхности, образовывала микропористую пленку, толщина которой контролировалась спектрально. Спектры регистрировали на ИК-Фурье спектрометре NICOLET 510 в интервале температур 77-273 К. В согласии с более ранними данными [1-4], в исходном спектре пленки льда наряду с мощными полосами поглощения при 3220 и 1620 cм -1 (2432 и 1210 cм-1 для D2O), принадлежащими водородно-связанным молекулам воды, присутствуют слабые полосы при 3696 (H2O) и 2728 (D2O) cм-1. Адсорбция CO, озона и этилена приводит к смещению этих полос в низкочастотную область, составляющему для полосы OD 33, 41 и 59 cм-1, соответственно (см. рис.1, кривые 1-4). Такое понижение частоты характерно для образования слабой водородной связи гидроксильных групп с адсорбированными молекулами. Как и следует ожидать, частоты самих адсорбированных молекул смещаются при этом незначительно. Так полоса адсорбированного CO наблюдается при 2154 cм-1, всего на 11 cм-1 выше, чем у свободных молекул в газовой фазе. Полосы адсорбированного озона возникают при 1107, 1034 и 704 cм-1 [6], как и в случае адсорбции на SiO2 [7], мало отличаясь от частот газообразного озона (1103, 1042 и 701 cм-1).Добавление озона в кювету с предварительно адсорбированным этиленом (или дейтероэтиленом) наряду с появлением полос поглощения озона приводит к уменьшению интенсивности полос этилена и возникновению новых максимумов, принадлежащих продуктам озонолиза. Среди последних можно выделить поглощение формальдегида (1720 см -1), а также полосы первичных и вторичных озонидов (рис. 1, кривые 5, 6). Менее стабильные первичные озониды (полосы 725 см-1, и др.) исчезают после повышения температуры до 150 K, остальные полосы сохраняются до более высоких температур.
Рис.1. Изменения в ИК спектре пленки льда D 2O (1) после адсорбции СО (2), О3 (3), этилена (4), после добавления озона к адсорбированному этилену (5) и повышения температуры до 220 K (6). Спектры 1-5 записаны при 77 K. Кривые 2-6 представляют собой разностные спектры, полученные после вычитания спектра исходной пленки (1).Полученные нами данные о спектрах адсорбированного озона были подтверждены в недавней статье [8]. Результаты работы демонстрируют применимость метода ИК-спектроскопии к исследованию адсорбции и механизма реакций адсорбированных газов на поверхности пористых пленок льда, которые можно рассматривать как систему, моделирующую атмосферные аэрозоли. Работа выполнена при поддержке конкурсного центра фундаментального естествознания Минобразования России (грант 9-177, и персональный грант конкурса молодых ученых). |
| (c) АСФ России, 2001 |